Кардиомиопатия у детей
Кардиомиопатия — это заболевание миокарда, приводящее к утолщению волокон миокарда или фиброзу.
Гипертрофическая кардиомиопатия характеризуется утолщением мышечных стенок желудочков, как правило, с участием желудочковой перегородки.
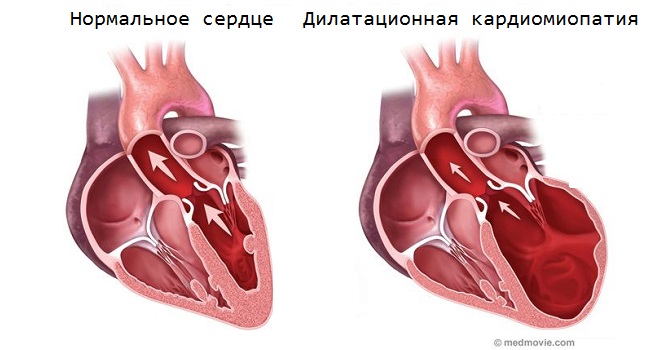
Дилатационная кардиомиопатия может также вызывать гипертрофию стенок желудочков, однако из-за сильного расширения желудочковых камер они кажутся тонкими и растянутыми.
Ключевые факты
- Дилатационная кардиомиопатия является наиболее распространенной формой кардиомиопатии. Это может быть конечным результатом миокардита. В большинстве случаев этиология неизвестна.
- Дилатационная кардиомиопатия вызывает слабый сердечный выброс и отек легких. Лечение включает в себя диуретики для снижения преднагрузки, инотропные средства для улучшения сократимости сердца и вазодилататоры, такие как ингибиторы АПФ, для снижения после нагрузки.
- Гипертрофическая кардиомиопатия является вторичной по отношению к генетическому заболеванию.
- Представление гипертрофической кардиомиопатии может включать аритмию, обморок, боль в груди или шум в сердце.
- Лечение гипертрофической кардиомиопатии включает уменьшение обструкции тракта оттока левого желудочка с помощью отрицательных инотропных агентов и контроль аритмий с помощью лекарств или имплантированного дефибриллятора.
- Ограничительная кардиомиопатия — это редкая форма кардиомиопатии. Симптомы связаны с системным венозным застоем и могут включать отек желудочно-кишечного тракта, приводящий к анорексии и плохому всасыванию.
Кардиомиопатия — это хроническое и прогрессирующее заболевание сердечной мышцы, которое может проявляться в различных формах, а в тяжелых случаях может привести к сердечной недостаточности и внезапной смерти. У детей в возрасте до года вероятность развития кардиомиопатии в десять раз выше, чем у детей в возрасте 2–18 лет. Гипертрофическая кардиомиопатия встречается в 5 случаях на миллион детей.
Патология
Гипертрофическая кардиомиопатия характеризуется аномальным ростом и расположением мышечных волокон, называемых мышечным расстройством. Процесс начинается в желудочках и в тяжелых случаях может включать стенку предсердия. Это может быть приобретено, вторично к вирусной инфекции или химиотерапии, или унаследовано как аутосомно-доминантное, аутосомно-рецессивное или Х-сцепленное заболевание, такое как синдром Барта. Кардиомиопатия также может быть вторичной по отношению к более распространенному метаболическому, митохондриальному или мультисистемному расстройству.
Кардиомиопатия в основном может быть разделена на два типа: ишемическая и неишемическая. Детская кардиомиопатия является почти исключительно неишемической, которая далее подразделяется Всемирной организацией здравоохранения на четыре типа в зависимости от типа повреждения мышц:
- Дилатационная кардиомиопатия (58%);
- Гипертрофическая (30%);
- Сдерживающая (5%);
- Аритмогенная правожелудочковая кардиомиопатия (5%).
Дилатационная кардиомиопатия чаще всего идиопатическая. Другие случаи вызваны вирусными инфекциями, такими как вирус Коксаки или ВИЧ, вторичными по отношению к токсинам, таким как доксорубицин, или связанными с тяжелой анемией или дефицитом питательных веществ.
При гипертрофической кардиомиопатии чаще всего левый желудочек является наиболее пораженной камерой с перегородкой, показывающей наибольший рост. Термин для этого явления — асимметричная гипертрофическая кардиомиопатия. Иногда утолщение может быть симметричным или концентрическим, охватывая всю стенку левого желудочка, или в редких случаях локализоваться на верхней стороне.
Аритмогенная правожелудочковая кардиомиопатия является чрезвычайно редким заболеванием у детей, при котором мышцы правого желудочка становятся дезорганизованными и замещаются фиброзной тканью. Начав с пятнистого поражения, процесс может постепенно распространяться на весь правый желудочек, а затем на левый желудочек. Дезорганизация клеток приводит к аритмиям и плохой сократимости.
Патофизиология
Дилатационная кардиомиопатия приводит к дилатации и плохой сократимости желудочков. Наблюдается прогрессирующая митральная и трикуспидальная регургитация. Со временем у пациента появляются признаки хронической сердечной недостаточности и гиперволемии.
Гипертрофическая кардиомиопатия вызывает ненормальное расслабление сердца во время диастолы и вторичную обструкцию венозного возврата. На терминальных стадиях этого заболевания сердце напоминает то, которое наблюдаются при дилатационной кардиомиопатии.
При рестриктивной кардиомиопатии наблюдается нормальная систолическая функция, но ненормальное расслабление. Желудочки становятся жесткими и плохо расширяются. Хотя желудочки не показывают увеличения, предсердия сильно увеличены. Приток крови к сердцу ограничен.
Клинические проявления
Кардиомиопатия не зависит от пола, расы, географии или возраста. Около 50–60% детей с гипертрофической кардиомиопатией и 20–30% с дилатационной кардиомиопатией имеют семейный анамнез. Симптомы гипертрофической кардиомиопатии могут впервые проявиться со всплеском роста в период полового созревания.
Клинические симптомы очень разнообразны и могут отсутствовать, быть легкими или серьезными. Общие симптомы, не специфичные для какого-либо одного типа кардиомиопатии, включают тахипноэ, плохой аппетит и задержку развития в младенчестве и плохую переносимость физической нагрузки у детей старшего возраста. Могут возникать желудочно-кишечные расстройства, такие как тошнота и рвота. Так же может быть гепатомегалия, отёк ног и хрипы в легких. Другие признаки могут включать шум в ушах, аритмии, боль в груди и обмороки.
При сдерживающей кардиомиопатии распространенные симптомы включают тахипноэ в состоянии покоя, легкую утомляемость, обморок, боль в груди или сухой кашель. Кардиомиопатия может быть связана с нарушением обмена веществ, которое может сопровождаться такими симптомами, как мышечная слабость, снижение мышечного тонуса, задержка роста, задержки развития, неспособность развиваться или постоянная рвота и вялость. Редко может быть инсульт или судороги. Также может быть связь с синдромом порока развития с дисморфическими особенностями, характерными для синдрома, такими как низкий рост и перепончатая шея, наблюдаемая при синдроме Нунан.
Диагностика
При любых подозрениях на кардиомиопатию следует обращаться к детскому кардиологу. Эхокардиограмма является наиболее широко используемым и наиболее информативным неинвазивным тестом для диагностики кардиомиопатии. С помощью эхокардиограммы практикующий врач может не только указать тип кардиомиопатии, но и определить степень дисфункции сердечной мышцы. С помощью эха можно измерить толщину стенки, фракцию выброса, размер камеры, степень обструкции, если есть, и регургитацию митрального или трикуспидального клапанов. Измерения давления в желудочках и магистральных сосудах, таких как легочная артерия, также могут быть выполнены. Регулярные эхокардиограммы необходимы для оценки прогресса заболевания. Кроме того, для оценки необходимы рентгенография грудной клетки, электрокардиограмма и холтеровский мониторинг в течение 24–72 часов. Рентген грудной клетки может показать кардиомегалию или плевральный выпот. ЭКГ может указывать на статус заболевания при отсутствии симптомов.
В некоторых случаях может возникнуть необходимость в более инвазивных тестах, таких как радионуклидная вентрикулограмма или катетеризация сердца. Радионуклидная вентрикулограмма может быть лучшим способом диагностики аритмогенной дисплазии правого желудочка (АДПЖ). Катетеризация сердца может быть необходима для выполнения мышечной биопсии. Это помогает в оценке возможных инфекций сердца и некоторых заболеваний обмена веществ. Биопсия может также идентифицировать жир в мышечной стенке или структурное повреждение желудочка для диагноза АДПЖ.
Определенные биохимические, генетические и ферментные тесты необходимы прежде, чем начинать наиболее подходящую медицинскую терапию. Особенно важно пройти метаболический скрининг у детей с кардиомиопатией в возрасте до 4 лет. Это может потребовать дополнительного анализа крови, мочи и тканей и консультации с такими специалистами, как генетики или неврологи.
Лечение
Медикаментозная терапия у ребенка с дилатационной кардиомиопатией направлена на достижение нескольких целей:
- Контроль симптомов застойной сердечной недостаточности с помощью таких препаратов, как ингибиторы АПФ и диуретики.
- Улучшение сократимости путем использования дофамина и добутамина у критически больных пациентов и дигоксина перорально в качестве поддерживающей терапии.
- Лечение или профилактика аритмий с помощью антиаритмиков, таких как амиодарон.
- Предотвращение образования тромбов с помощью антикоагулянтов, таких как аспирин или варфарин.
Лечение, специфичное для ребенка с гипертрофической кардиомиопатией, включает в себя:
- Контроль симптомов, связанных с обструкцией, с помощью блокаторов кальциевых каналов или бета-блокаторов, таких как верапамил и пропранолол.
- Улучшение наполнения камер сердца.
- Профилактика аритмий и внезапной смерти с помощью антиаритмических средств, таких как амиодарон или дизопирамид.
Пациентам с сопутствующими нарушениями обмена веществ может потребоваться тщательный диетический мониторинг жиров, избегание голодания и возможный ежедневный прием перорального карнитина.
Имплантация кардиостимулятора может рассматриваться для мониторинга или стабилизации брадикардии. Было показано, что двухкамерная стимуляция уменьшает обструкцию оттока при гипертрофической кардиомиопатии. Автоматический внутренний кардиовертер-дефибриллятор рекомендуется в случаях серьезных аритмий, угрожающих жизни, обморока или истории реанимации после остановки сердца.
Миэктомия — это хирургическое удаление части утолщенной перегородочной мышцы, которая блокирует кровоток при гипертрофической кардиомиопатии. Несмотря на то, что она может контролировать симптомы сердечной недостаточности, вторичной по отношению к обструкции, исследования не показали, что эта процедура предотвращает внезапную смерть от аритмий или останавливает прогрессирование заболевания.
Трансплантация сердца является последним средством, когда пациенты достигают конечной стадии заболевания. Около 20% детей с симптомами кардиомиопатии нуждаются в пересадке сердца в течение первого года жизни.
Экстракорпоральная мембранная оксигенация (ЭКМО) может использоваться для поддержания критических пациентов, пока не будет доступен подходящий орган. Кроме того, дети весом более 50 кг имеют право на поддержку с помощью устройства под названием «Система поддержки левого желудочка» в течение примерно 3–12 месяцев.
В дополнение к пациенту все родственники первой степени должны проходить скрининг с помощью эхокардиограммы и ЭКГ каждые 1-3 года до 12 лет и чаще до 21 года. Те, у кого в анамнезе была кардиомиопатия в семье и у которых отсутствуют симптомы, могут проходить скрининг раз в 5 лет. Если установлен конкретный генетический диагноз, все братья и сестры должны быть генетически протестированы для оценки их риска.
Прогноз
Общий прогноз зависит от типа кардиомиопатии и возраста первого диагноза. До 40% детей с диагнозом кардиомиопатия не проходят лечение в течение первого года после постановки диагноза. Смертность и частота пересадки сердца намного выше у детей с кардиомиопатией по сравнению со взрослыми. Для тех детей, которые приобретают кардиомиопатию, вторичную по отношению к вирусной инфекции, 33% выздоравливают, 33% стабилизируются и 33% испытывают прогрессирование своего заболевания. В настоящее время 5-летняя выживаемость у детей с диагнозом гипертрофическая кардиомиопатия составляет 85–95%, а при дилатационной кардиомиопатии — 40–50%. В случаях сдерживающей кардиомиопатии выживаемость в течение 2 лет составляет 44–50%. Внезапные сердечные смерти составляют 50% смертей при гипертрофической кардиомиопатии и 28% при сдерживающей кардиомиопатии.